Anvisa atualiza status de desenvolvimento das vacinas contra a Covid-19; Veja
Veja qual vacina está em status mais avançado no Brasil e saiba se já existe a solicitação para o uso emergencial de cada laboratório.
A Anvisa, desde ontem (15), passou a divulgar o status das análises preliminares para registro, autorização emergencial e outras informações sobre o desenvolvimento de vacinas contra a Covid-19 no Brasil.
Confira o andamento da submissão de documentos apresentados pelas empresas desenvolvedoras. Sempre que houver mudanças no cenário, os dados desta página serão atualizados.
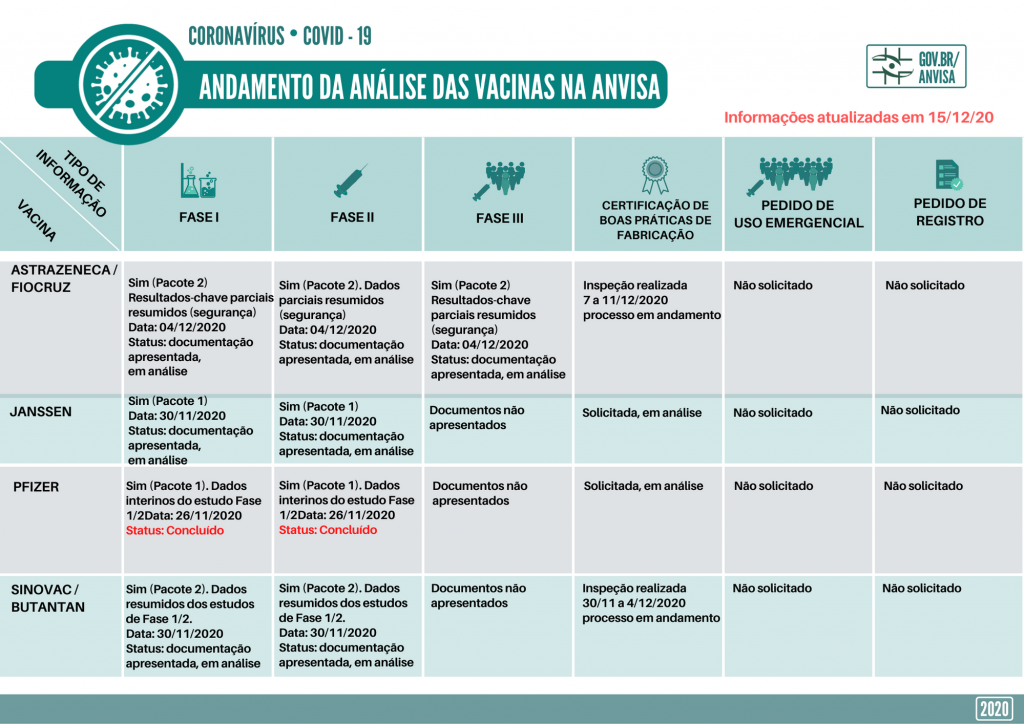
Cada fase da Anvisa
Fase 1 – essa é a primeira etapa de testes em humanos para avaliar a segurança e possíveis reações indesejáveis no local da aplicação da vacina ou no organismo. Nessa fase também pode ser verificada, de forma preliminar, a imunogenicidade da vacina, ou seja, sua capacidade de gerar anticorpos contra o novo coronavírus.
Fase 2 – é hora de avaliar a dose, a forma de vacinação e a capacidade de gerar anticorpos (contra o novo coronavírus) na população (faixa etária, por exemplo) que deverá ser indicada para receber a vacina. A segurança continua em análise aqui.
Fase 3 – os testes nessa etapa são realizados em grandes populações para avaliar a segurança e a eficácia da vacina. A vacina precisa provar que, de fato, é capaz de nos proteger da doença.
Pedido de uso emergencial – feito antes do registro final para aplicar a vacina em um grupo específico da população. Precisa ser enviado à Anvisa pela empresa fabricante ou importadora da vacina, presente no território brasileiro. Pode ser realizado com a fase 3 em andamento. Saiba mais sobre esse tipo de pedido.
Registro – profissionais especializados da Agência vão revisar todos os documentos técnicos e regulatórios e verificar os dados de segurança e eficácia, bem como avaliar a qualidade da vacina. O registro concedido pela Anvisa é o sinal verde para que a vacina seja comercializada e disponibilizada no país. Precisa ser solicitado à Anvisa pela empresa fabricante da vacina.
Dados de eficácia e segurança: essas informações compreendem estudos clínicos e não clínicos. Estão incluídos aqui dados referentes aos estudos realizados em animais e humanos.
Dados de tecnologia farmacêutica: são dados referentes à qualidade, ao processo de fabricação e ao controle de qualidade. Eles têm como objetivo demonstrar que o produto será fabricado com qualidade e de forma consistente, dentro das especificações de uso. Esses dados também determinam o prazo de validade do produto.
Pacotes: são grupos de documentos apresentados pelas empresas à Anvisa.
Pacotes 1, 2, 3 e sucessivamente: são pacotes com dados e informações parciais. As empresas apresentarão mais dados e informações em pacotes subsequentes ou quando apresentarem o pedido de registro da respectiva vacina.
Status: é referente à análise de um determinado pacote de documentos.
Submissão parcial: assim chamada porque a empresa não apresentou a documentação completa para o registro da respectiva vacina.
Certificação de Boas Práticas de Fabricação: avaliação realizada por inspetores qualificados para garantir que uma fábrica, em qualquer lugar do mundo, cumpre com os requisitos determinados pela legislação brasileira.
São avaliadas as estruturas físicas das áreas de produção, armazenamento e laboratórios de controle de qualidade, além de toda a documentação do sistema de garantia de qualidade da empresa. (Com assessoria)


Comentários estão fechados.